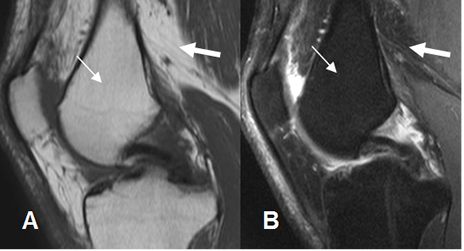
Fig 1. Medula ósea en adulto normal
A: RM sagital en T1 y B: RM sagital en STIR. La señal de la medula osea amarilla (Flecha delgada), es similar a la de la grasa (Flecha gruesa).
VALORACION RADIOLOGICA.
En el capítulo de médula ósea, se hace una mas amplia descripción de los hallazgos normales y patológicos.
Para resumir la medula ósea contiene tanto células hematopoyéticas, como grasas. El predominio de cada una determina si es roja o amarilla.
La imagen normal de la medula amarilla en T1 y STIR es similar a la grasa subcutánea. (8). (Fig 1 y 2).
La medula roja en T1 tiene una señal intermedia menor que la grasa, pero más alta que el músculo. (8). (Fig 3).

Fig 1. Medula ósea en adulto normal
A: RM sagital en T1 y B: RM sagital en STIR. La señal de la medula osea amarilla (Flecha delgada), es similar a la de la grasa (Flecha gruesa).
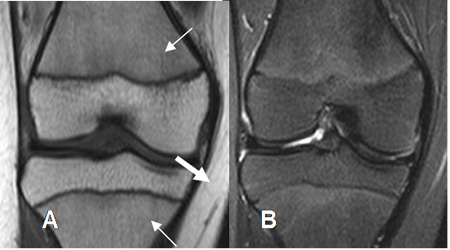
Fig 2 Medula ósea en niño normal
A: RM coronal en T1 y B: RM coronal en STIR. Medula osea amarilla en la epífisis distal del fémur y proximal de la tibia. Medula osea roja en las metafisis con señal intermedia (Flechas delgadas), menor que la grasa. (Flechas gruesas).
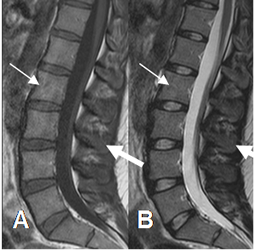
Fig 3. Medula ósea roja normal.
A: RM sagital en T1 y B: RM sagital en T2. Medula con señal intermedia en ambas secuencias (Flechas delgadas), mas alta que el músculo. (Flechas gruesas).
Aún con el avance y desarrollo de las diferentes modalidades diagnósticas, la radiografía (Rx) simple sigue siendo la modalidad de elección para el estudio inicial de este tipo de patología. (2). Permite localizar la lesión y determinar su tamaño, bordes, reacción perióstica, calcificación, etc. Con estos hallazgos, se puede hacer la primera impresión.
Es posible identificar una lesión lítica, se cuando ha comprometido mas del 30 al 50% de la mineralización osea. (6). (Fig 4A).
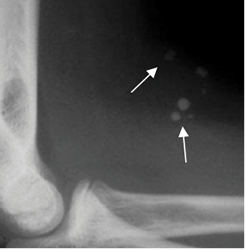
Fig 4A. Calcificaciones en los tejidos blandos.
Rx lateral. Prominencia de los tejidos blandos de la parte anterior del codo, con calcificaciones que corresponden a flebolitos, por un hemangioma.
Una lesión focal puede corresponder a metástasis de un tumor conocido o no, especialmente en pacientes de edad avanzada. (6).En estos casos, la gamagrafía es la modalidad de elección, para determinar si es única o múltiple o encontrar lesiones ocultas. Tiene alta sensibilidad para detectar lesiones con actividad osteoblástica, antes que la Rx, con excepción de tumores renales, de tiroides y el mieloma. (2, 6). (Fig 4B).
La gamagrafía también permite determinar la actividad de una lesión, que puede ser benigna o maligna. Por lo general una baja actividad, descarta la malignidad y el paso de una lesión inactiva a una activa, sugiere transformación maligna. (2).
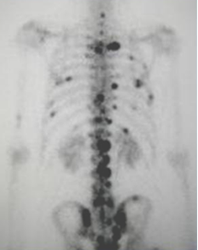
Fig 4 B. Gamagrafía ósea.
Enfermedad metastásica con múltiples focos de aumento en la actividad, de predominio en la columna, costillas y pelvis.
La ecografía es una prueba mas barata y accesible que otras modalidades. Es de primera elección en la valoración de masas de tejidos blandos y sobre todo en los niños. (9).
Su principal valor es que permite diferenciar entre una lesión quística y sólida. En muchas ocasiones no se encuentra una alteración anatómica y la comparación con la extremidad contralateral ayuda bastante. (10). (Fig 5).
En algunas lesiones benignas como lipomas, hemangiomas, quistes y cuerpos extraños, los cambios son suficientes y no requieren de otras pruebas. Para otras lesiones sólidas, los hallazgos son inespecíficos y se requieren de otros estudios. (9).
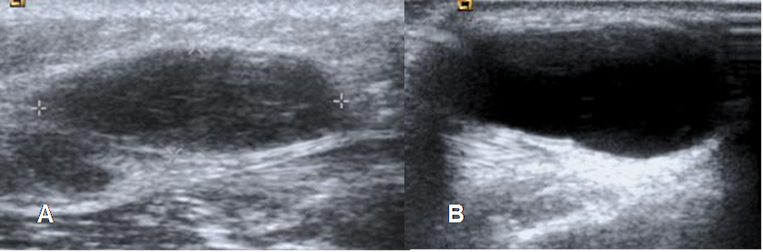
Fig 5. Diferenciación lesiones en ecografía.
A y B: Ecografía. Lesión sólida que corresponde a lipoma en A y lesión quística, que produce reforzamiento posterior en B, por quiste de baker.
La tomografía axial computarizada (TAC) está indicada, ante la duda de ruptura de la cortical, valorar las características de las calcificaciones y estudiar sitios de difícil visualización por interposición de estructuras, como la pelvis, el hombro y la región paraespinal. (4, 5). (Fig 6, 7 A y B).
Además sirve como guía para realizar estudios intervencionistas, como toma de biopsias percutáneas y terapias ablativas. (2). (Fig 8).
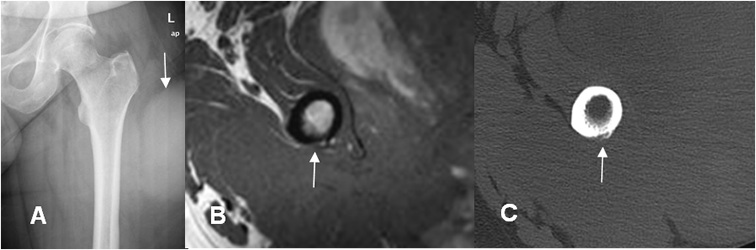
Fig 6. Invasión cortical.
A: Rx AP. No se encuentran anormalidades óseas. Prominencia de los tejidos blandos de predominio en la parte lateral del muslo, por proceso neoplásico.
B: RM axial en T1. Patología neoplásica de crecimiento agresivo y que cruza compartimientos. Se encuentra adelgazamiento en la cortical posterior del fémur, existiendo sospecha de invasión ósea.
C: TAC axial en ventana ósea. Erosión cortical secundaria a compromiso óseo, de un tumor de tejidos blandos.
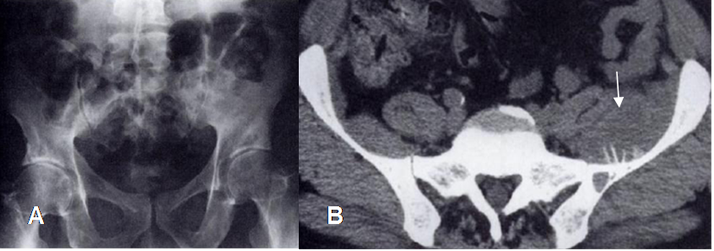
Fig 7 A. Tumor no visto en la pelvis.
A: Rx AP. Interposición de gas intestinal en la pelvis, que limita la valoración.
B: TAC axial. Lesión lítica del iliaco, con reacción perióstica y masa de tejidos blandos, por osteosarcoma, que no puede ser detectada en la Rx simple.
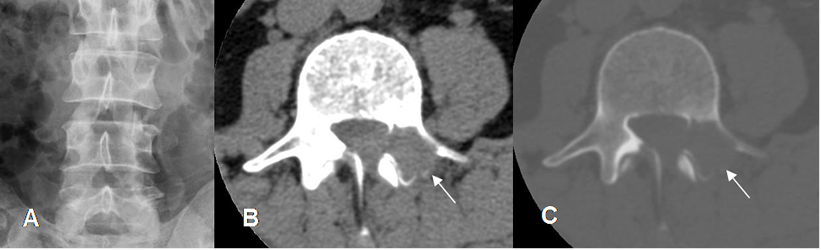
Fig 7 B. Tumor no visto en columna.
A: Rx AP. No se aprecian alteraciones.
B: TAC axial en ventana de tejido y C: TAC axial en ventana osea. Lesión lítica y expansiva en la lámina y el pedículo, no demostrada en la Rx simple.
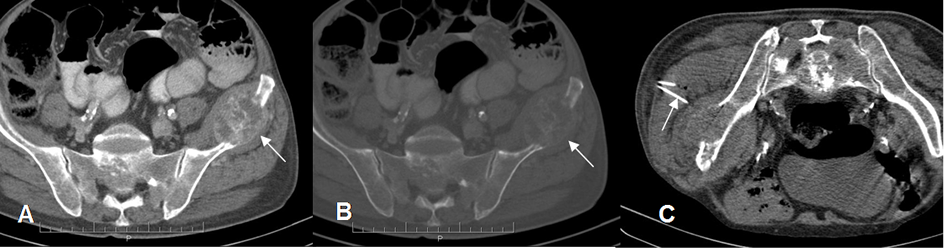
Fig 8. Guía de procedimiento con TAC.
A y B: TAC axial. Lesión lítica con masa de tejidos blandos, en el iliaco izquierdo, por metástasis de tumor broncogénico.
C: TAC axial en Prono. Toma de biopsia por vía glútea. Aguja: Flecha delgada.
La resonancia magnética (RM) es la modalidad de elección, para caracterizar los tumores óseos. Permite hacer el estadiaje local, por su buena capacidad multiplanar y su resolución, para valorar los tejidos blandos. (2, 4, 5).
La RM es muy sensible pero poco específica, ya que la mayoría de lesiones son hipointensas en T1 e hiperintensas en T2 y STIR, por el alto contenido de agua. (2, 5). (Fig 9).
Algunas lesiones pueden tener áreas hiperintensas en T1 por el contenido de grasa, sangrado subagudo (metahemoglobina), líquido con alto contenido de proteínas o la presencia de melanina. (2).Las lesiones con alto contenido fibroso, pueden ser hipointensas o de señal intermedia en T2 y en lesiones quísticas se puede encontrar un nivel líquido/líquido. (2). (Fig 10 y 11).
En lesiones con presencia de calcificaciones gruesas o sangrado crónico (hemosiderina), se produce un efecto de susceptibilidad magnética produciendo imagen hipointensa en gradiente eco (GE). (2).
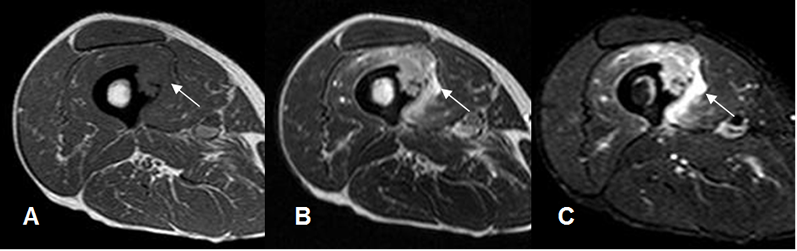
Fig 9. Lesión en RM.
A: RM axial en T1, B: RM axial en T2 y C: RM axial en STIR. Lesión de tejidos blandos en el muslo, que compromete la cortical, hipointensa en T1, hiperintensa en T2 y STIR.
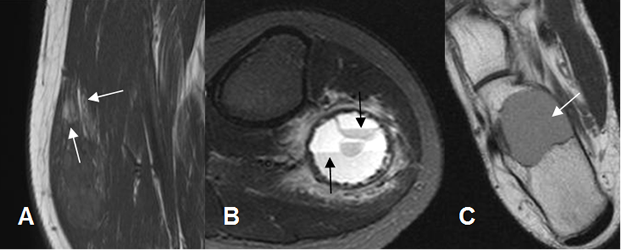
Fig 10. Hallazgos en RM.
A: RM sagital en T1. Masa de tejidos blandos en la parte anterior del muslo, con zona hiperintensa, que corresponde a sangrado subagudo de un hemangioma.
B: RM axial en STIR. Niveles líquido/líquido, en un quiste óseo aneurismático de la cabeza del peroné.
C: RM axial en T1. Lesión quística de señal intermedia, por alto contenido de proteínas en un quiste óseo.

Fig 11. Lesiones fibrosas en RM.
A: RM sagital en T1, B: RM sagital en T2 y C: RM sagital en STIR. Múltiples lesiones redondeadas e hipointensas en todas las secuencias, por enfermedad metastásica de mama, con alto contenido fibroso.
Se recomienda que una imagen con sospecha de malignidad en RM, no sea interpretada sin correlacionar con una Rx simple. (8).
El uso de contraste (Gadolinio) sigue siendo limitado y controvertido. La diferenciación del tumor con tejido sano, puede hacerse en secuencias de T2, sin necesidad de utilizarlo, aunque puede aportar datos sobre el grado de vascularización. (5, 6).
Esta diferencia tiene poco valor práctico, porque se considera parte de la lesión y debe ser resecado. (5).
El contraste es útil para identificar zonas de tumor sólido, componente quístico, necrosis y hemorragia, lo que permite planificar la toma de biopsia y valorar el compromiso articular. (5, 6). (Fig 12 y 13).
También se utiliza para identificar la extensión intra-articular y en el seguimiento después de cirugía, radio o quimioterapia y determinar la recidiva tumoral. (3).
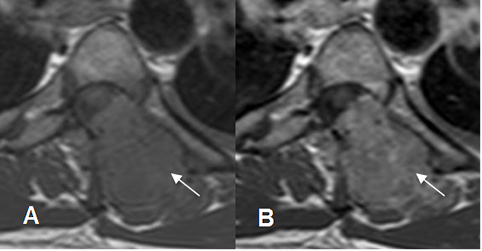
Fig 12. Contraste en RM.
A: RM axial en T1 simple y B: RM axial en T1 con contraste. Enfermedad metastásica pulmonar, con gran masa de tejidos blandos paraespinal y en la parte posterior izquierda del canal, que presenta realce homogéneo del contraste.

Fig 13. Contraste en RM.
A: RM axial en T1 simple y B: RM axial en T1 con contraste. Lesión metastásica que compromete el sacro, con masa de tejidos blandos. Hay realce heterogéneo del contraste, que indica zona de necrosis central. (Flechas).
La tomografía por emisión de positrones (PET), es una nueva técnica funcional, que valora el metabolismo de una lesión. (2).
Se utiliza la F-deoxiglucosa (FDG) como marcador, existiendo con una alta correlación entre la captación y la agresividad del tumor.
El PET es muy utilizado para el seguimiento post-quirúrgico, detectar recurrencia local o enfermedad metastásica. Es muy útil en casos donde el material metálico produce artefactos en la RM o TAC, que limitan la valoración. Igualmente se utiliza para evaluar la respuesta de quimioterapia adyuvante, en sarcomas. (2). (Fig 14).
Tiene la desventaja de mostrar bastantes falsos positivos por lesiones benignas o no neoplásicas, como osteomielitis, enfermedad de Paget, displasia fibrosa, fibroma no osificante, quiste óseo simple, artritis reumatoidea, sarcoidosis, nódulos pulmonares benignos, etc. (2).
El PET es superior a la gamagrafía para detectar metástasis líticas o mixtas, mieloma múltiple o metástasis de sarcoma de Ewing y tiene baja sensibilidad en metástasis blásticas, como las de próstata. (2).
Por el contrario un PET negativo ante un nódulo pulmonar sospechoso, no puede descartar una metástasis. (2).

Fig 14. Tomografía por emisión de positrones.
A: TAC axial y B: PET axial. Lesiones metastásicas en los alerones del sacro. (Flechas delgadas). Hay otras lesiones en ambos iliacos, no detectadas con el TAC, pero con aumento del metabolismo en el PET. (Flechas gruesas).
Para hacer la aproximación diagnóstica inicial, se debe tener en cuenta:
La mayoría de los tumores tienen una distribución por edad y localización característica, aunque se encuentran excepciones. (4). El tumor de células gigantes aparece cuando se han cerrado los núcleos de crecimiento y los quistes óseos aneurismáticos rara vez se desarrollan después de los 20 años. (3). En personas de edad avanzada, deben considerarse inicialmente tumores malignos primarios o metastáticos.
La toma de biopsia es otro aspecto muy importante. El conocimiento de la anatomía compartimental evita resecciones óseas amplias y en ocasionas permite salvar la extremidad. (15).
El abordaje debe planificarse conjuntamente con el cirujano, para no contaminar otros compartimientos, ni lesionar estructuras neurovasculares. Adicionalmente, el trayecto de la aguja debe ser resecado junto con el tumor primario, en casos de malignidad. (6, 15).
Cuando se encuentran varias lesiones, debe escogerse la que menos riesgo tenga para la toma de biopsia (15), teniendo en cuenta que la vía mas corta y directa, puede no ser la mejor. (7).
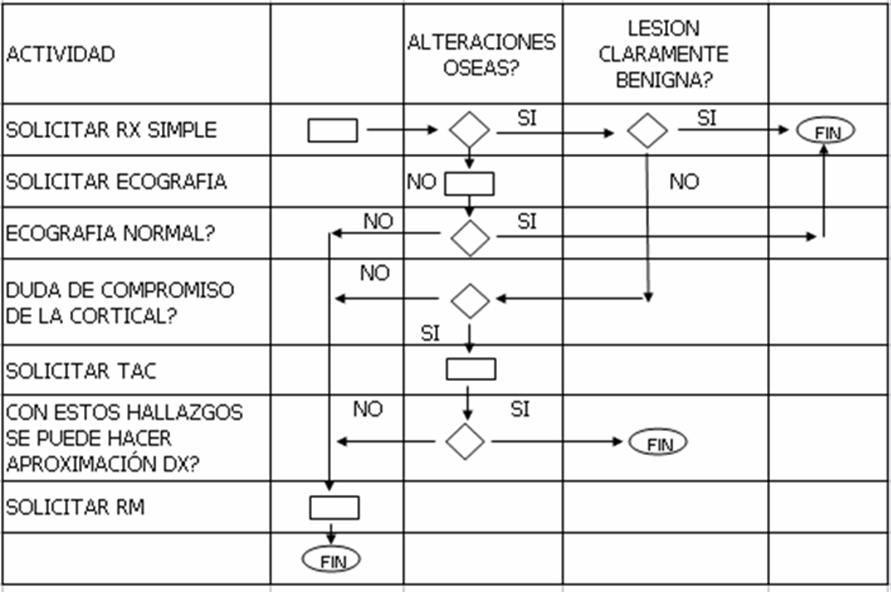
Algoritmo propuesto para el estudio de tumores osteomusculares:
Iniciar la evaluación con Rx simple. (6).
Con la integración de todas las modalidades hacer la aproximación diagnostica, el estadiaje local y corporal.
Posteriormente discutir el manejo y la toma de biopsia con el cirujano, en los casos que este indicado.
| Fecha de creación | Marzo 1 de 2011 |
| Fecha de actualización | Marzo 5, 2015 |